38. Карбонові кислоти
Естери
Визначення. Естери – це похідні кисневмісних кислот, у яких гідроксигрупи кислоти заміщені залишками спирту або фенолу.
Загальна формула естерів органічних кислот:
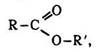
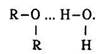
де R, R` – вуглеводневі радикали.
Класифікація. Розрізняють естери органічних та мінеральних кислот (азотної, сірчаної, фосфорної тощо). Серед естерів дво- чи багатоосновних кислот є кислі та середні.
Номенклатура. Вживається ще така загальна назва естерів – складні ефіри. Назви естерів походять від назв кислот і спиртів (або фенолів). Так, естер з формулою ![]() має назви етилметаноат, етилформіат, етиловий ефір форміатної (мурашиної, метанової) кислоти, мурашиноетиловий ефір, з формулами С2H5–О–SО3Н і С2Н5–О–SO2–О–С2H5 – етилгідрогенсульфат і диетилсульфат, з формулою
має назви етилметаноат, етилформіат, етиловий ефір форміатної (мурашиної, метанової) кислоти, мурашиноетиловий ефір, з формулами С2H5–О–SО3Н і С2Н5–О–SO2–О–С2H5 – етилгідрогенсульфат і диетилсульфат, з формулою 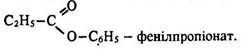
Ізомерія. Для сетерів характерна ізомерія кислотних та вуглеводневих радикалів, а також міжкласова – з карбоновими кислотами. Так, ізомером етилетанату 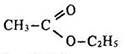 є бутанова кислота С3Н7–СООН.
є бутанова кислота С3Н7–СООН.
Будова молекули. Молекули сетерів складаються з двох структурних елементів – радикалів кислоти та спирту (чи фенолу). Атом кисню, що їх з’єднує, походить від спирту (або фенолу).
Поширення в природі. Естери дуже поширені в природі. Багато з них входить до складу ефірних масел і обумовлює приємний запах квітів, плодів і ягід. Естери триатомного спирту гліцерину та вищих жирних кислот є основою жирів, а вищих одноатомних спиртів та монокарбонових жирних кислот – воску та спермацету.
Фізичні властивості. Естери нижчих карбонових кислот і спиртів – безбарвні леткі рідини з приємним фруктовим запахом. Оцтово-ізоаміловий естер має запах груші, масляно-бутиловий – ананасу. Естери мінеральних кислот – маслянисті рідини з приємним запахом, вищих спиртів і вищих карбонових кислот – тверді речовини, що майже не мають запаху. Вони мало розчинні у воді і добре – в спирті та інших органічних розчинниках.
Температури плавлення та кипіння сетерів нижчих спиртів менші, ніж у відповідних кислот.
Хімічні властивості. Найважливішою хімічною властивістю сетерів є їх взаємодія з водою – гідроліз або омилення. Якщо естер, наприклад оцтово-етиловий, нагрівати з водою за наявності неорганічної кислоти (або лугу), утворюються оцтова кислота (чи її сіль) та етиловий спирт:
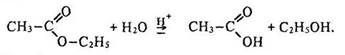
Гідроліз естерів – процес, протилежний реакції етерифікації:
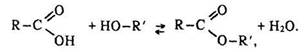
Щоб змістити рівновагу праворуч, точно в бік утворення естеру, треба за принципом Ле Шательє взяти в надлишку вихідну кислоту або спирт, відігнати естер, що утворюється, або видалити воду. Луг необоротно зміщує рівновагу в бік гідролізу, оскільки зв’язує кислоту, утворюючи сіль:
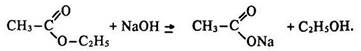
Одержання. Природні естери екстрагують з рослин органічними розчинниками. Промисловий спосіб їх добування базується на реакції етерифікації:
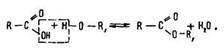
Слід пам’ятати, що в цій реакції вода утворюється з гідроксигрупи кислоти та атома водню спирту.
Використання. Естери застосовують як розчинники у харчовій промисловості (для приготування фруктових есенцій), косметиці, медицині (ізоамілнітрат, етилнітрат).