32. Алкіни
Алкіни
Визначення. Ацетиленові вуглеводні – це ненасичені аліфатичні вуглеводні, що мають один потрійний зв’язок. Вони утворюють гомологічний ряд з загальною формулою СnН2n–1, де n > 2.
Номенклатура. Вживають таку назву ацетиленових вуглеводнів: алкіни. Назви окремих речовин утворюють з назв алканів заміною суфікса -ан на -ин чи -ін (табл. 58).
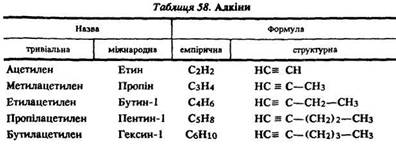
Ізомерія. В алкінів (починаючи з бутину) спостерігається структурна ізомерія, обумовлена розгалуженням вуглецевого ланцюга або положенням потрійного зв’язку в ньому. Наприклад, пентин утворює такі ізомери:
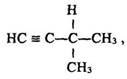
пентин-1 НСºС–СН2–СН2–СН3, 3-метилбутин-1, ізомерія якого спричинена розгалуженням ланцюга вуглецевих атомів пентин-2, ізомерія якого обумовлена зміною положення потрійного зв’язку: СН3–СºС–СН2–СН3.
Слід звернути увагу, що у алкінів немає просторових цис- і транс-ізомерів, оскільки не існує двох різних замісників у атома вуглецю, який зв’язаний потрійним зв’язком.
Алкіни, в яких число атомів вуглецю перевищує три, мають ізомери серед алкадієнів.
Будова молекули. Розглянемо будову алкінів на прикладі ацетилену. Відстань між атомами вуглецю в ньому (0,12 нм) менша, ніж в етилені, кут між зв’язками дорівнює 180°. Молекула ацетилену має лінійну будову (рис. 30).
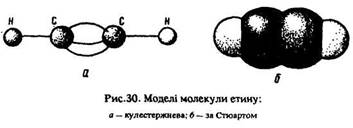
Атоми вуглецю в ацетилені розташовані ближче, ніж у етилені внаслідок утворення другого пі-зв’язку. Вони зв’язані потрійним зв’язком, що складається з одного сигма- і двох пі-зв’язків, розміщених у взаємно перпендикулярних площинах. Збільшення кута до 180° (в етилені 120°) відбувається внаслідок sр-гібридизації, в якій, на відміну від етилену, беруть участь одна рx-орбіталь і одна s-орбіталь кожного атома вуглецю.
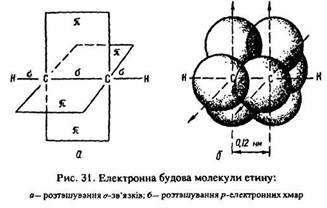
Електрони py і рz-орбіталей, що утворюють два пі-зв’язки, не гібридизуються. У результаті sр-гібридизації в ацетилені кожний атом вуглецю має дві гібридних sр-орбіталі. Ці орбіталі беруть участь в утворенні одного сигма-зв’язку між атомами вуглецю і одного сигма-зв’язку з s-орбіталлю атома водню. Молекула ацетилену має п’ять зв’язків: три сигма-зв’язки (один sр–sр між атомами вуглецю, два sр–s між атомами вуглецю та водню) і два пі-зв’язки між атомами вутлецю (рис. 31).
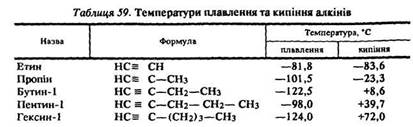
Фізичні властивості. Перші три члени гомологічного ряду алкінів – гази, алкіни від С4 до С8 – рідини, наступні – тверді речовини (табл. 59).
Хімічні властивості. Хімічні властивості алкінів і алкенів подібні. Для них характерні реакції приєднання, окислення та полімеризації. Однак, на відміну від алкенів, реакція приєднання у алкінів відбувається в дві стадії (спочатку розривається один пі-зв’язок і утворюються похідні алкенів, потім другий – утворюються похідні алканів), можливі також реакції заміщення. Розглянемо хімічні властивості алкінів на прикладі ацетилену. Реакції приєднання. Гідрогенізація. Реакція відбувається у дві стадії – спочатку утворюється етилен, потім – етан:
![]()
Галогенування. Реакція з бромною водою протікає за звичайних умов, також у дві стадії:
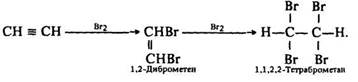
Під час пропускання ацетилену крізь бромну воду вона знебарвлюється. Це–якісна реакція на алкіни і всі ненасичені вуглеводні.
Приєднання галогеноводнів. Реакція відбувається за правилом Марковникова (Т = 120–180 °С) за наявності каталізаторів – активованого вугілля або НgCl2:
![]()
Гідратація. Реакція відбувається за наявності каталізаторів – солей ртуті (II):
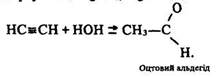
Оцтовий альдегід – важлива хімічна сировина, з нього виробляють пластмасу, етиловий спирт, оцтову кислоту. Реакцію гідратації ацетилену називають реакцією Кучерова на честь російського вченого М. Кучерова, який відкрив її у 1881 р.
Окислення. Ацетилен може окислюватися. Водний розчин перманганату калію КМnО4 знебарвлюється під час пропускання крізь нього ацетилену:
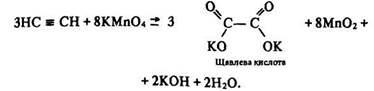
У кисні ацетилен горить сліпучим полум’ям з виділенням великої кількості теплоти:
![]()
Цю реакцію застосовують для зварювання та різання металів.
Тримеризація. Під час пропускання ацетилену крізь розжарене вугілля (Т = 800 °С) утворюється бензол:
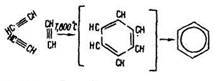
Димеризація. За наявності солей міді (І), які є каталізатором, ацетилен димеризується у вінілацетилен:
![]()
Вінілацетилен є важливим проміжним продуктом виробництва хлоропренового каучуку.
Кислотні властивості. На відміну від етану та етилену ацетилен виявляє властивості кислот, атоми водню в ньому можуть заміщуватися на атоми металу. Так, під час пропускання ацетилену крізь аміачні розчини солей срібла або міді утворюються осади ацетиленідів:
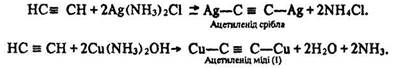
Ацетиленіди міді та срібла вибухають від удару. Ацетиленідом є також карбід кальцію:
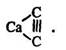
Під дією кислот на ацетиленіди виділяється ацетилен:
![]()
Кислотні властивості ацетилену можна пояснити більшою полярністю зв’язків С–Н порівняно з етиленом і етаном.
Згідно з сучасною теорією будови речовини, чим більша частка з-орбіталей атома вуглецю в утворенні ст-зв’язку, тим міцніше він притягує до себе електронні пари сусідніх зв’язків, тобто тим полярніший зв’язок С–Н (табл. 60).

Тому найменша полярність зв’язку С–Н в етані, найбільша – в ацетилені.
Одержання ацетилену. У промисловості і в лабораторних умовах ацетилен добувають:
а) з метану:
![]()
б) з карбіду кальцію (під час розкладу карбіду кальцію водою):
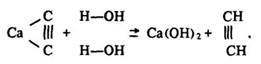
Використання ацетилену. Ацетилен є вихідною речовиною для виробництва багатьох хімічних сполук: етилового спирту, оцтової кислоти, синтетичного каучуку, хлорвінілових і поліхлорвінілових пластмас.