4. БУДОВА АТОМА
4. БУДОВА АТОМА
4.4. Поведінка електрона в атомі
Сьогодні поведінка електрона в атомі пояснюється законами квантової механіки, в основи якої лежать такі основні положення:
- Електрон має подвійну (корпускулярно-хвильову) природу – може поводити себе як частинка (має масу і заряд) і як хвиля (характерні явища дифракції та інтерференції).
- Для електрона неможливо визначити точне положення в просторі у певний момент часу. Можна говорити лише про ймовірність перебування його у тій чи іншій частині простору.
Частина простору навколо ядра, у якій ймовірність перебування електрона становить понад 90% називається електронна орбіталь. Цей простір обмежується поверхнею і є об’ємною геометричною фігурою.
Розглянемо для прикладу атом Гідрогену, у якого навколо ядра обертається лише один електрон. Якщо фотографічно фіксувати положення електрона в атомі Гідрогену у різні моменти, то одержуємо картину, зображену на рис. 4.3.
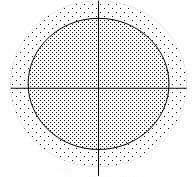
Рис. 4.3. Схематичне зображення електронної орбіталі.
Простір, де зафіксовано найбільше кількість точок обмежений сферою – це орбіталь, на якій розміщений електрон. Її іноді називають електронною хмарою. Однак, іноді електрон може знаходитись і поза межами орбіталі (з ймовірністю до 10%).
У квантовій механіці для зручності орбіталь позначають квадратиком або горизонтальною рискою і називають електронною або квантовою коміркою, а електрон позначають вертикальною стрілкою (↑ або ↓). Запис ![]() або
або ![]() означає, що на орбіталі розміщений один електрон.
означає, що на орбіталі розміщений один електрон.