10. ОСНОВИ ЕЛЕКТРОХІМІЇ
10. ОСНОВИ ЕЛЕКТРОХІМІЇ
10.2. Електроліз
У розглянутих вище редокс-реакціях процес окиснення завжди супроводжувався процесом відновлення. Будь-яка з них може використовуватись у ГЕ для генерації електричного струму. Постає запитання “Чи можливий зворотній процес – перетворення електричної енергії у хімічну?”
Такі процеси реалізуються при проходженні постійного електричного струму через систему з двох електродів, під’єднаних до джерела струму і занурених у розплав або розчин електроліту.
Реакції, що відбуваються під дією постійного електричного струму в розчинах або розплавах електролітів називають електролізом. Електроліз здійснюють у приладах – електролізерах (рис. 10.2).
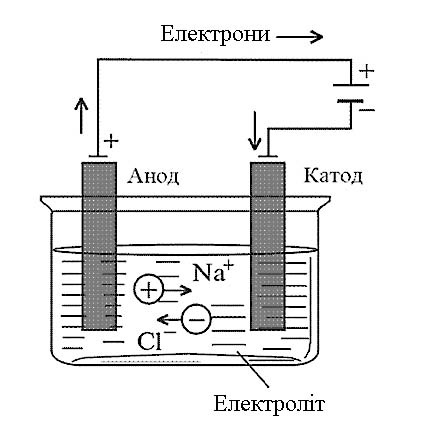
Рис.10.2. Схема електролізу розплаву NaCl.
Розглянемо докладніше деякі випадки електролізу.