11. РОЗЧИНИ
11. РОЗЧИНИ
11.4. Залежність розчинності речовин від різних факторів
Розчинність визначається трьома факторами: природою розчинника, природою розчиненої речовини (агрегатний стан) і зовнішніми умовами (температура, а для газів і тиск).
Вплив природи розчинника і розчиненої речовини виражається правилом “подібне розчиняється в подібному”. Полярні та іонні сполуки добре розчиняються в полярних розчинниках (вода, спирти, ДМФА), а неполярні (прості речовини, вуглеводні) – у неполярних (вуглеводні, тетрахлорметан). Так, галогеноводні (полярні молекули) добре розчинні у воді (полярний розчинник), але погано розчинні у бензені (неполярний розчинник). З іншого боку, у воді не розчиняються галогенпохідні вуглеводнів (тетрахлорметан, дихлоретан), які добре розчинні у бензені.
Вплив температури. Зі зростанням температури, розчинність більшості речовин зростає, а при зниженні – зменшується. Часто тверді речовини розчиняють при нагріванні, а потім при охолодженні розчину частина їх викристалізовується. Такий метод використовують для очистки речовин і називають кристалізацією.
Якщо гарячий насичений розчин обережно охолоджувати, то розчинена речовина може не кристалізуватись. Утворюється пересичений розчин. Пересичені розчини нестійкі і навіть при незначному струшуванні починається спонтанна кристалізація. Теж саме спостерігається при внесенні кристалика речовини (“затравки”) у її пересичений розчин, або терті скляною паличкою до стінок посудини, що веде до утворення центрів кристалізації. Легко утворюють пересичені розчини кристалогідрати натрій тіосульфату Na2S2O3∙5H2O, натрій тетраборату (бура) Na2B4O7∙10H2O, натрій сульфату Na2SO4∙10H2O.
Існують речовини, розчинність яких зі зростанням температури зменшується. Це, зокрема, кальцій гідроксид Са(ОН)2, кальцій сульфат CaSO4. Залежність розчинності речовин від температури зображається кривими розчинності (рис. 11.2).
За кривими розчинності можна знайти коефіцієнт розчинності і масу кристалів, що утворюються при охолодженні розчину в певному інтервалі температур.
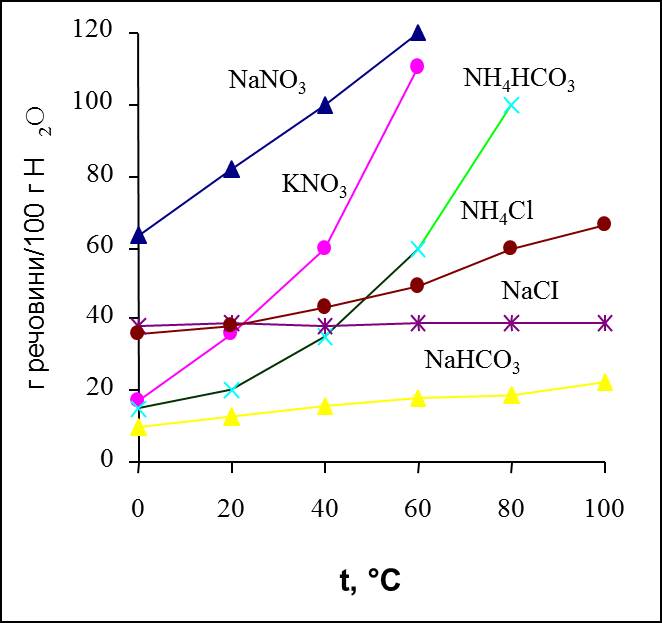
Рис.11.2. Залежність розчинності деяких солей від температури.
Як і для твердих тіл, розчинність рідин у рідинах зі зростанням температури зростає. Температура, вище або нижче якої речовини необмежено розчинні одна в одній, називається критичною. Так, для системи вода – фенол критичною є температура 66,4 0С, нижче якої вони обмежено розчинні один в одному, а вище – необмежено.
Розчинність газів у рідинах зі зростанням температури зменшується. Гази, що не утворюють сполук з розчинником, погано розчиняються у ньому (табл. 11.1). Як видно з табл. 11.1, гази, що не утворюють сполук з водою (азот N2, кисень O2) дуже мало у ній розчинні. Якщо ж процес розчинення супроводжується утворенням хімічної сполуки (H2CO3, HCl + HClO, NH3∙H2O), то розчинність помітно зростає.
Таблиця 11.1
Розчинність деяких газів у воді при різних температурах
|
Газ |
Температура, 0С |
||||
|
0 |
20 |
40 |
60 |
||
|
не взаємодіють з водою |
N2 |
0,024 |
0,016 |
0,012 |
0,01 |
|
O2 |
0,049 |
0,031 |
0,023 |
0,019 |
|
|
взаємодіють з водою |
CO2 |
1,713 |
0,878 |
0,530 |
0,360 |
|
Cl2 |
4,60 |
2,30 |
1,48 |
1,24 |
|
|
HCl |
525 |
440 |
390 |
340 |
|
|
NH3 |
1176 |
702 |
405 |
214 |
|
Вплив тиску спостерігається лише на розчинність газів і непомітний при розчиненні рідин чи твердих речовин. Зі зростанням тиску розчинність газів збільшується. Кількісно це описується законом Генрі: при сталій температурі розчинність газу Х в рідині прямо пропорційна його парціальному тиску:
СХ = КХрХ
де СХ – концентрація газу в насиченому розчині, моль/л;
КХ – стала Генрі для газу Х, моль∙л–1∙Па–1;
рХ – парціальний тиск газу Х на розчином, Па.
Закон Генрі справедливий лише для газів, що не взаємодіють з розчинником.
Взаємний вплив розчинених речовин. Якщо у деякому розчиннику вже розчинені певні речовини, то інші речовини в ньому розчиняються гірше. Найсильніше на це впливають електроліти, що пояснюється сольватацією іонів, яка в свою чергу веде до зменшення концентрації вільних молекул розчинника. Та частина молекул розчинника, яка зв’язана з іонами електроліту, не є розчинником для інших речовин.
Кількісно розчинність твердих речовин характеризується коефіцієнтом розчинності ks – відношення маси речовини mB у насиченому при даній температурі розчині до маси розчинника mS:
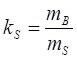
Розчинність S – максимальна маса речовини mB, г, яка може розчинитись у 100 г розчинника за даних умов:
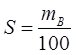
За здатністю до розчинення розрізняють легкорозчинні (більше 10 г речовини на 100 г води), малорозчинні (0,01 – 1 г), важкорозчинні (до 0,01 г) (табл. 11.2). Абсолютно нерозчинних речовин не існує.
Таблиця 11.2
Розчинність речовин
|
|
Розчинність при 20 0С |
Кількісні параметри |
Приклад |
|
Речовини |
добре розчинні |
> 10 г речовини в 100 г Н2О |
35,8 г натрій хлориду NaCl в 1 л Н2О |
|
малорозчинні |
від 10–3 г до 10 г речовини в 100 г Н2О |
0,17 г кальцій гідроксиду Са(ОН)2 в 1 л Н2О |
|
|
практично нерозчинні |
< 10–3 г речовини в 100 г Н2О |
2,3∙10–4 г барій сульфату BaSO4 в 1 л Н2О |