13. ОСНОВНІ КЛАСИ НЕОРГАНІЧНИХ РЕЧОВИН
13. ОСНОВНІ КЛАСИ НЕОРГАНІЧНИХ РЕЧОВИН
13.1. Класифікація неорганічних речовин
Усі відомі речовини умовно можна розділити на прості та складні. Простих речовин (з урахуванням алотропних модифікації) відомо біля 400. Усі прості речовини поділяють на метали і неметали.
Складні речовини можуть мати неорганічну або органічну природу. Неорганічні речовини класифікують за кількістю елементів, що утворюють сполуки – двоелементні (бінарні), триелементні та багатоелементні. Класифікацію органічних речовин розглянуто у розд. Органічна хімія.
Схема 13.1
Класифікація неорганічних речовин
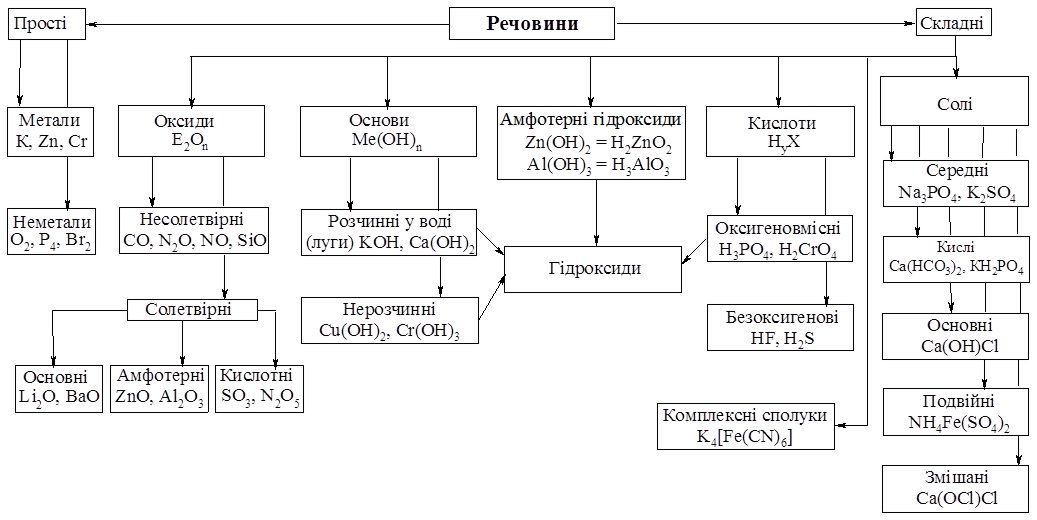
Бінарні – сполуки утворені атомами двох елементів. Сполуки металів із неметалами класифікують за типом неметалу (табл. 13.1). Сполуки металів з металами називають інтерметалічними (інтерметалідами).
Таблиця 13.1
Класифікація бінарних сполук за типом неметалу
|
Неметал |
Клас |
Формула |
Назва |
|
F, Cl, Br, I |
галогеніди |
KF, FeBr3 |
калій фторид, ферум (ІІІ) бромід |
|
О |
оксиди, пероксиди |
CaO, Nа2O2 |
кальцій оксид, натрій пероксид |
|
S, Se, Te |
халькогеніди |
ZnS, Li2Se |
цинк сульфід, літій селенід |
|
N, P, As |
пніктогеніди |
Na3N, Mg3P2 |
натрій нітрид, магній фосфід |
|
C |
карбіди |
СаС2, Al4C3 |
кальцій карбід, алюміній карбід |
|
Si |
силіциди |
Mg2Si |
магній силіцид |
|
B |
бориди |
Сa3B2 |
кальцій борид |
|
Н |
гідриди |
NaH |
натрій гідрид |
Найважливішими бінарними сполуками є галогеніди, які можна розглядати як солі відповідних безоксигенових кислот та оксиди (схема 11.1).
Гідроліз бінарних сполук веде до утворення відповідних гідрогеновмісних сполук неметалів та гідроксидів:
FeBr3 + 3H2O = Fe(OH)3↓ + 3HBr; Na2O + H2O = 2NaOH;
Al2S3 + 6H2O = 2Al(OH)3↓ + 3H2S; Mg3N2 + 6H2O = 3Mg(OH)2↓ + 2NH3;
CaH2 + H2O = Ca(OH)2↓ + H2; CaC2 + 2H2O = Ca(OH)2↓ + C2H2;
Гідроліз деяких бінарних сполук відбувається необоротно.
Триелементними сполуками є основи, кислоти і деякі солі. Багатоелементними – комплексні сполуки, серед яких виділяють основи, кислоти, солі та неелектроліти.