35. Спирти
Етиленгліколь і гліцерин
Етиленгліколь і гліцерин – перші представники гомологічних рядів дво- та триатомних насичених спиртів:
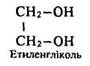
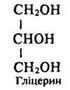
У всіх багатоатомних спиртах гідроксигрупи знаходяться біля різних атомів вуглецю. Одержати спирт з двома гідроксигрупами біля одного атома вуглецю неможливо – така сполука нестійка, як і вугільна кислота
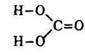
яка існує лише у водному розчині.
Етиленгліколь та гліцерин – безбарвні сиропоподібні рідини, солодкуваті на смак, добре розчинні у воді. Етиленгліколь – отрута. Гліцерин – гігроскопічна, неотруйна речовина, що легко засвоюється організмом.
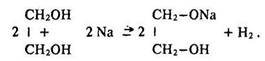
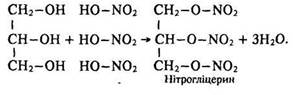
Під час взаємодії з органічними та мінеральними кисневмісними кислотами утворюються складні ефіри:
Як сполуки, що містять гідроксигрупи, багатоатомні спирти за властивостями подібні до одноатомних спиртів. Натрій витісняє з них водень:
Нітрогліцерин – важка масляниста рідина, що вибухає від легкого струсу або внаслідок нагрівання. Він застосовується в медицині, а також для виготовлення динаміту. При взаємодії гліцерину з вищими карбоновими кислотами утворюються жири.
Разом з тим багатоатомні спирти мають властивості, відмінні від властивостей одноатомних спиртів. Кілька гідроксигруп, що виявляють негативний індукційний ефект, взаємно впливають одна на одну, внаслідок чого посилюється рухливість їх атомів водню. В ряду первинних спиртів (одноатомні – двоатомні – триатомні) кислотні властивості посилюються. Ступінь дисоціації гліцерину в десять разів більший, ніж метанолу. Тому на відміну від одноатомних спиртів багатоатомні легко взаємодіють з лугами та з гідроксидом міді (II), утворюючи алкоголяти:
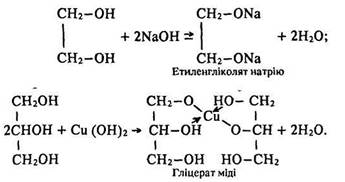
Етиленгліколят та гліцерат міді – комплексні сполуки. Стрілками у формулі гліцерату міді показані хімічні зв’язки, які виникли за донорно-акцепторним механізмом. Здатність багатоатомних спиртів реагувати з гідроксидами важких металів пояснюється на лише їх підвищеною кислотністю, але й утворенням стійких комплексних сполук з ними. Алкоголяти міді (II) , одержані з багатоатомних спиртів, мають яскраво-синій колір. Взаємодія багатоатомних спиртів з гідроксидом міді (II) – якісна реакція на багатоатомні спирти.
Багатоатомні спирти добувають взаємодією галогенопохідних відповідних вуглеводнів з водним розчином лугу:
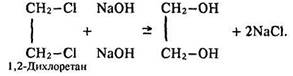
Гліцерин одержують гідролізом жирів, а також синтетичним способом з газів крекінгу нафти. Реакція промислового добування гліцерину за останнім способом має такий вигляд:
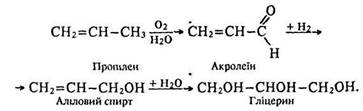
Водні та спиртові розчини етиленгліколю та гліцерину застосовують для виготовлення антифризів – розчинів, що не замерзають за низьких температур. Вони є замінниками води і радіаторах авто- та авіамоторів.
Етиленгліколь застосовують для одержання лавсану - цінного синтетичного волокна, гліцерин – для добування синтетичних смол і вибухових речовин, наприклад нітрогліцерину.
Гліцерин є гігроскопічною речовиною. В медицині він використовується для пом’якшення шкіри рук і виготовлення мазей у шкіряному виробництві – для запобігання висиханню шкір, текстильній промисловості – для надання тканинам м’якості та еластичності.